Dioxyde de carbone : Différence entre versions
m (orthographe) |
(→Liens externes) |
||
| Ligne 41 : | Ligne 41 : | ||
* [[Stockage géologique du CO2]] | * [[Stockage géologique du CO2]] | ||
| − | + | == Liens externes == | |
| + | * [http://www.dpe-diagnostic-performance-energetique.eu/dpe.php Calcul de l'empreinte carbonne avec le DPE.] | ||
===Bibliographie=== | ===Bibliographie=== | ||
[[Catégorie:Composé chimique]][[Catégorie:Polluant]] | [[Catégorie:Composé chimique]][[Catégorie:Polluant]] | ||
Version du 24 juin 2010 à 19:54
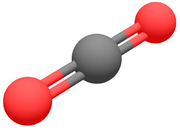
Le dioxyde de carbone est un composé chimique composé d'un atome de carbone et de deux atomes d'oxygène et dont la formule brute est: CO2.
Cette molécule linéaire a pour formule développée de Lewis: O=C=O
Dans les conditions normales de température et de pression Le dioxyde de carbone est un gaz incolore communément appelée gaz carbonique.
C'est un gaz à effet de serre.
Il est produit notamment lors de la fermentation aérobie ou de la combustion de composés organiques, et lors de la respiration des animaux et des végétaux. Pour ces derniers, la photosynthèse piège beaucoup plus de CO2 que ce que la respiration en produit.
Sommaire
Histoire
Le chimiste Jan Baptist van Helmont ( médecin belge ) décrivit le premier le dioxyde de carbone en 1638
Utilisation
Le dioxyde de carbone sous forme solide est utilisé pour:
- refroidir des denrée périssables.
- refroidir des denrée périssables.
Sous forme gazeuse, il est utilisé pour:
- carbonater des boissons (soda ou eau),
- créer une couche isolante (flux) dans l'industrie alimentaire ou pour la soudure,
- stimuler la croissance des plantes
- solubiliser le calcaire dans l'eau de distribution.
Sous forme liquide, il est utilisé comme:
- réfrigérant pour congeler certains aliments,
- réfrigérant dans l'industrie électronique,
- agent d'extinction dans les extincteurs dit au dioxyde de carbone,
- agent propulseur (et parfois également carbonatant) pour les boissons servies à la pression.
Sa présence peut-être détectée grâce à de l'eau de chaux